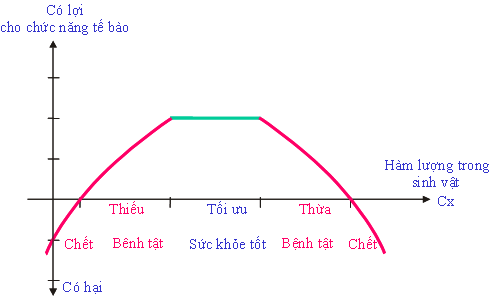
Hình 1. Ảnh hưởng của các mức hàm lượng
nguyên tố (Cx) đối với chức năng tế bào
và tình trạng sức khoẻ
của con người.
ĐỊA HÓA NGUYÊN TỐ FLUOR VÀ VAI TRÒ
ĐỐI VỚI SỨC KHỎE CỘNG ĐỒNG Ở
VIỆT
QUÁCH ĐỨC TÍN1, ĐOÀN
THỊ NGỌC HUYỀN1, NGUYỄN THỊ MINH NGỌC2,
NGUYỄN VĂN LUYỆN1, NGUYỄN HỒNG QUANG1, MAI TRỌNG TÚ1
1Viện Khoa học Địa chất và
Khoáng sản; Thanh Xuân, Hà Nội
2Trường
Đại học Khoa học Tự nhiên, ĐHQG HN; Nguyễn
Trãi, Thanh Xuân, Hà Nội
Tóm tắt:
Fluor (F) là nguyên tố vi lượng cần
thiết cho cơ thể sống. Theo tiêu chuẩn vệ
sinh nước ăn uống của Bộ Y tế
(1329/2002/BYT/QĐ), hàm lượng F chấp nhận
được là 0,7 mg/l <F
<1,5 mg/l. Nếu cơ thể con
người hấp thụ quá nhiều hoặc quá ít F từ
môi trường, thì sẽ dẫn đến những tác
động có hại cho sức khỏe, như gây nên
các bệnh về răng và xương (bệnh thừa-thiếu
fluor - fluorosis). Ngoài ra, còn có thể bị suy giảm hoạt
động của tuyến giáp hoặc gây tổn
thương tới não.
Kết quả nghiên cứu ở Việt
Nam cho thấy, hàm lượng F trong các loại thực phẩm
không cao. Một số địa phương có biểu hiện
thiếu hụt F trong môi trường nước như Hà
Nội, Lạng Sơn và đồng bằng Cửa Long.
Trong khi đó, có những vùng hàm lượng F rất cao,
điển hình là trong nước dưới đất ở
Vạn Ninh, Ninh Hòa, Cam Ranh, tỉnh Khánh Hòa và một số
vùng khác của các tỉnh Thái Bình, Bình Định và Ninh Thuận.
Để bảo vệ sức khỏe
cộng đồng, cần xác định rõ vùng nào thừa,
vùng nào thiếu, để có biện pháp tối ưu nhằm
bổ sung hoặc loại bỏ F trong nước sinh hoạt
và thực phẩm. Do vậy, nghiên cứu tổng thể
nhằm đánh giá hành vi địa hóa và sự phân bố tự
nhiên của F trong môi trường địa chất là cần
thiết và cần sớm triển khai. Bài báo này chỉ ra
những tồn tại trong nghiên cứu và một số
định hướng trong chương trình hành động
liên quan đến F trên lãnh thổ Việt
I. GIỚI THIỆU
Fluor (F) là nguyên tố rất cần
thiết cho cơ thể sống; sự dư thừa hoặc
thiếu hụt F trong môi trường đều ảnh
hưởng xấu đến sức khoẻ của con
người (Hình 1). Biểu hiện rõ rệt nhất là các
bệnh thừa-thiếu fluor (fluorosis) tác động đến
xương và răng.
Bệnh thừa-thiếu fluor
là một bệnh địa phương khá phổ biến
ở nhiều vùng trên thế giới như Ấn Độ,
Trung Quốc, Thái Lan, Mỹ, Anh, Tây Ban Nha, … Ở nước
ta, cũng đã có một số vùng có biểu hiện
địa phương về loại bệnh này. Điển
hình là các vùng Vạn Ninh, Cam Ranh ở tỉnh Khánh Hòa, Tây
Sơn, An Nhơn ở tỉnh Bình Định và một số
vùng ở các tỉnh Ninh Thuận và Thái Bình.
Sự phân bố và tác động
của F tới sức khỏe của cộng đồng
bước đầu đã được một số
tổ chức và nhà khoa học Việt Nam nghiên cứu,
trong đó, đáng kể nhất là kết quả điều
tra của Viện Vệ sinh Tp Hồ Chí Minh về sự
phân bố của F trong một số nguồn nước
của đồng bằng Cửu Long. Ngoài ra, còn có kết
quả khảo sát hàm lượng F trong nước uống
và thực phẩm ở Hà Nội của Võ Thế Quang
[14], hàm lượng F trong nước uống ở vùng Ninh
Hòa (Khánh Hòa) của Đặng Trung Thuận [1] và vùng Vạn
Ninh (Khánh Hòa) của Đặng Trung Thuận và Đặng
Trung Tú [2], Đỗ Thị Vân Thanh [3] và Nguyễn Đình
Hòe [5]. Tuy nhiên, vẫn chưa có các nghiên cứu một cách
toàn diện về sự phân bố của F trong các hợp
phần môi trường tự nhiên và đánh giá những
tác động bất lợi của sự dư thừa
hoặc thiếu hụt F tới sức khỏe và sự
phát triển của cộng đồng dân cư.

Hình 1. Ảnh hưởng của các mức hàm lượng
nguyên tố (Cx) đối với chức năng tế bào
và tình trạng sức khoẻ
của con người.
Để hạn chế
được những tác hại và phát huy mặt có ích của
F, cần nghiên cứu hành vi địa hoá của nó trong môi
trường tự nhiên, bao gồm nghiên cứu về nguồn
gốc, sự phân bố, hành vi, cơ chế xâm nhập
vào môi trường, tác hại của F đến con
người và hệ sinh thái, từ đó đưa ra giải
pháp hạn chế tác động có hại và giải quyết
triệt để ô nhiễm môi trường gây ra bởi
F.
II. ĐẶC
ĐIỂM ĐỊA HÓA CỦA NGUYÊN TỐ FLUOR
Fluor
được nhà hoá học người Pháp Henri Moisson phát
hiện năm 1886. Trong bảng hệ thống tuần
hoàn, F có số thứ tự thứ 9, nằm ở nhóm
VIIA, chu kỳ 2 cùng với các nguyên tố khác của nhóm
halogen bao gồm chlor, brom và iod.
F khá phổ
biến trong thiên nhiên, với hàm lượng trung bình trong vỏ
Trái đất theo Vinogradov [12] là 0,6%. Fluor thường gặp
ở trạng thái khí F, có màu xanh vàng nhạt, mùi hắc, vị
cay, là chất độc cực mạnh, nếu hít phải
sẽ bị tổn thương niêm mạc. F có nguyên tử
lượng là 18,998; tỷ trọng 1,8.10-3 g/cm3
(ở 200C), nhiệt độ đông đặc
219,60C; nhiệt độ sôi là -188,4 0C, cấu
hình electron của nguyên tử F ở trạng thái khí: [He]1s22s22p5,
bán kính nguyên tử = 0,71 Å. Bán kính ion F- = 1,33 Å. Thế
ion hoá đầu tiên của F = 17,422eV, độ điện
âm = 4.
Fluor có một đồng vị bền
là 19F và 12 đồng vị không bền liên tục
từ 15F đến 27F.
1. Tính linh động
trong môi trường
Fluor có hoạt tính hóa học mạnh,
độ linh động cao trong tất cả các môi
trường từ môi trường oxy hóa đến môi
trường khử, từ môi trường kiềm - trung
tính đến môi trường axit. Vì thế, khí F phản ứng
với hầu hết các vật chất hữu cơ và vô
cơ trừ khí trơ và nitơ, khi phản ứng với
kim loại tạo muối fluorur và hòa tan vào nước tạo
thành axit fluorydric (HF).
Fluor là nguyên
tố có hoạt tính hoá học mạnh, nhưng các hợp
chất của F lại có độ tan không cao như các hợp
chất của chlor. Các muối fluorur phổ biến là
fluorur natri và fluorur calci. Fluorur natri hòa tan mạnh trong nước,
nhưng fluorur calci lại ít hòa tan. Fluor có khả năng tạo
nhiều hợp chất khá bền và ít bị thuỷ phân
(hợp chất với Al, Si, Fe, Ca, Mg, B,..). Do đó, sự
phân bố của F và các hợp chất của nó trong các
điều kiện môi trường khác nhau khá khác nhau về
hàm lượng và dạng tồn tại.
2. Dạng tồn
tại của fluor trong tự nhiên
Fluor ít tồn tại ở dạng
đơn chất mà thường ở trạng thái ion hoặc
kết hợp với các nguyên tố hóa học khác trong
khoáng vật. Các khoáng vật độc lập của F gồm:
fluorit (CaF2), topaz (Al2SiO4(F,OH)2),
cryolit (Na3AlF6). Fluor cũng tham gia vào các
khoáng vật khác như: mica, amphibol, fluorit, tourmalin, apatit,
villiaumit, fluorapatit, ... Trong các dạng tồn tại trên của
F, chỉ có 2 loại có giá trị công nghiệp là fluorit và
apatit.
3. Mối quan hệ
của fluor với các nguyên tố khác
Fluor là một hợp phần
tự nhiên của thủy quyển, thạch quyển, khí
quyển và sinh quyển. Sự tồn tại của F trong
môi trường phụ thuộc vào các điều kiện
của môi trường (Eh, pH, đặc điểm địa
chât, khí hậu,…) và mối tương tác với các nguyên tố
khác. Sự tương tác đó có quy luật hoặc không
rõ quy luật.
a. Quan hệ của fluor với calci và nhôm: Fluor có tương quan chặt chẽ với calci và
nhôm trong đất cũng như trong nước. Calci và
nhôm được coi là barie địa hóa chủ yếu của
F. Hàm lượng của calci và nhôm trong đất càng cao
thì lượng F tích tụ trong đất cũng càng cao.
Ngược lại, trong nước hàm lượng calci và
nhôm càng cao thì hàm lượng F toà tan trong nước sẽ
càng thấp.
b. Quan hệ của
fluor với các nguyên tố khác: Fluor thường kết hợp với
các nguyên tố hoá học khác trong các khoáng vật. Các tổ
hợp cộng sinh nguyên tố tự nhiên của F gồm:
+ F-Ca-Fe-S-Si-Ba-Sr-Pb-Zn-Cu trong các
mạch nhiệt dịch;
+ F-Al-Ca-Sn-Mo-W trong các mỏ
greisen;
+ Ta-P-F-Ti-REE (rare earth elements -
nguyên tố đất hiếm) trong các mỏ carbonatit;
+ F-U-V-Se-As-REE trong các mỏ
phosphorit;
+ Pb-Zn-Ba-F và
Sb-Hg-F trong các mỏ nhiệt dịch.
III. NGUỒN GỐC
CỦA FLUOR VÀ CÁC HỢP CHẤT CỦA NÓ TRONG TỰ NHIÊN
Nguồn cung
cấp F và các hợp chất của nó được chia
thành 2 loại là nguồn tự nhiên và nguồn nhân tạo.
1. Nguồn tự
nhiên
Thạch quyển
là nguồn cung cấp F chủ yếu cho thủy quyển,
thổ nhưỡng và khí quyển thông qua các quá trình hoạt
động địa chất nhiệt dịch, phong hóa,
núi lửa hoặc thông qua các đứt gãy kiến tạo.
Hoạt
động nhiệt dịch liên quan với các đá magma và
phun trào axit là một quá trình vận chuyển F từ một
nguồn dưới sâu lên gần mặt đất để
hình thành các mỏ fluorit nhiệt dịch trong điều kiện
địa chất thuận lợi, đồng thời tạo
nên các nguồn nước khoáng silic-fluor nóng và phát tán F vào
môi trường nước dưới đất. Các
đứt gãy sâu, các đới dập vỡ kiến tạo
là những kênh truyền dẫn nước có F.
Các nguồn
nước khoáng, nước nóng có thể vận động
ngầm theo các hệ thống đứt gãy, khe nứt
trong các đá mang theo F có trong đá và phát tán F ra xung quanh (các
nguồn nước nóng ở Đồng Xuân, Phú Yên chứa
hàm lượng F cao 16-17 mg/l).
Các hoạt
động núi lửa cũng cung cấp F cho khí quyển
(HF chiếm 2,5% thể tích khói núi lửa ở Hawai). Bởi
vậy, trong các vùng hoạt động núi lửa cổ và
hiện đại thì nước, đất và đá
thường giàu F. Hàm lượng F trong các hợp phần
của các vùng này cũng như vùng có nước nóng kiềm,
vùng có vỏ phong hoá trên mỏ fluorit, quặng phosphorit,
apatit,... đều giàu F hơn các vùng khác, chẳng hạn
nước dưới đất ở đây có thể chứa
tới n.10-2 - n.10-3 gF/l.
Quá trình phong
hoá các đá, đặc biệt là đá magma axit, quặng
F, quặng phosphorit giải phóng, hoà tan F trong đá hoặc
quặng đi vào nước, làm cho nguồn nước từ
vỏ phong hoá đá axit có hàm lượng F rất cao.
Nước
mưa cũng là nguồn cung cấp F đáng kể cho
đất, vỏ phong hoá, nước mặt, đặc
biệt là vùng cảnh quan ẩm lạnh (mùa mưa của
nhiều vùng thuộc Đông Âu chứa F khoảng n.10-4
- n.10-5 g/l, ở Nhật Bản khoảng 8,9.10-5
g/l). Lượng F đi vào đất bằng con
đường này tới 2 mg/100 m2. Chỉ một
phần nhỏ F được đưa về biển từ
vỏ phong hoá và nước mặt. Hàm lượng F trong
nước biển khoảng 0,8 - 1,4 mg/l. Dạng tồn tại
chủ yếu của F trong nước biển là F-.
Fluor dễ dàng bị hấp phụ và kết hợp với
các phân tử apatit, keo sét..., làm cho nước biển nghèo
F đi, nhưng bùn biển lại giàu F lên (bùn biển Thái
Bình Dương chứa 0,047% F, ở biển Đen là 0,054
% F). Nguồn F trong nước biển chủ yếu là hoạt
động núi lửa (trên cạn và dưới biển).
Trong lịch sử Trái đất, những giai đoạn
hoạt động mạnh của núi lửa (giai đoạn
tạo núi) và thời kỳ khô hạn đặc trưng bởi
sự làm giàu F trong môi trường.
2. Nguồn nhân
tạo
Các hoạt
động nhân sinh góp phần phát tán F mạnh vào môi trường
thông qua các hoạt động: khai thác, chế biến, sử
dụng fluorit và các hợp chất giàu F; các ngành công nghiệp
như sản xuất phân đạm, luyện gang thép, nhiệt
điện, xi măng, gạch ngói, …và các hoạt động
nông nghiệp sử dụng phân đạm làm tăng hàm
lượng F trong đất.
IV. SỰ PHÂN BỐ
CỦA FLUOR TRONG MÔI TRƯỜNG
1. Fluor trong
đá và vỏ phong hoá
Thạch quyển là nguồn
cung cấp F chính cho môi trường thông qua các quá trình hoạt
động địa chất. Hàm lượng trung bình
(ppm) của F trong thạch quyển là 660 và trong các đá
khác nhau được dẫn ra trong Bảng 1. Hàm lượng
trung bình của F trong các loại đá magma tăng dần từ
đá siêu mafic đến đá axit.
Bảng 1. Hàm
lượng trung bình của F trong các hợp phần của
vỏ Trái đất [12].
STT
|
Nhóm
|
Hợp phần
|
Hàm lượng
(ppm) |
|
1 |
|
Vỏ lục địa |
525 - 585 |
|
2 |
|
Thạch quyển |
660 |
|
3 |
|
Thiên thạch (chondrit) |
28 |
|
4 |
Đá
magma |
Đá siêu mafic |
100 |
|
5 |
Đá bazơ (gabbro, bazan) |
370 |
|
|
6 |
Đá
trung tính (diorit, andesit) |
500 |
|
|
7 |
Đá
axit (granit, granodiorit) |
800 |
|
|
8 |
Đá
trầm tích |
Syenit |
120 |
|
9 |
Sét |
740 |
|
|
10 |
Cát kết |
270 |
|
|
11 |
Carbonat |
330 |
|
|
12 |
Trầm tích nước sâu |
Đá
vôi |
540 |
|
13 |
Sét |
130 |
|
|
14 |
|
Than
đá |
50 |
Nước ta có trữ lượng
khoáng chất chứa F khá phong phú, chủ yếu nằm
trong quặng apatit và fluorit, tập trung ở khu mỏ
apatit, fluorit ở Lào Cai, Lai Châu và một lượng nhỏ
ở Xuân Lãnh, Phú Yên, …
Trong quá trình phong hóa, ở điều kiện môi
trường nhiệt đới, F được giải
phóng từ các khoáng vật chứa chúng, nhưng ít
được giữ lại trong lớp thổ nhưỡng
mà phần lớn được đưa vào nước
ngầm. Các hợp chất hữu cơ hòa tan, thúc đẩy
sự di chuyển và phát tán F từ đất, vỏ phong
hoá vào môi trường nước. Sự có mặt của
calci cản trở sự di chuyển F trong môi trường
khô hạn và vỏ phong hoá đá vôi, làm cho đất và vỏ
phong hoá ở đây giàu F hơn so với các hợp phần
khác. Trong vỏ phong hóa, F có thể bị hấp thụ bởi
oxit nhôm tạo kết tủa. F cũng bị rửa lũa
từ tầng mùn và tích tụ ở tầng tích lũy phía
dưới. Hàm lượng F trong nước sông, hồ
vùng nhiệt đới (<3.10-4 g/l) thường
nhỏ hơn so với vùng khô hạn (> 4.10-4 g/l),
do hàm lượng F trong đất và vỏ phong hoá cao
hơn và có hiệu ứng bay hơi.
2. Fluor trong
đất và thực vật
Fluor trong môi trường đất
đến từ nhiều nguồn khác nhau, cả nguồn
tự nhiên lẫn nguồn nhân tạo. Nhưng F ít
được giữ lại trong đất, mà dễ dàng
bị phát tán vào môi trường nước vì độ
hoà tan của F trong đất cao. Mức độ F tập
trung trong đất phụ thuộc vào lượng sét,
độ pH và hàm lượng của calci và nhôm. Một
lượng lớn F tập trung trong phần sét của
đất. Hàm lượng trung bình của F trong đất
là 200 ppm [12]. Những vùng nào mà F trong đất có hàm lượng
trên 500 ppm được xem là vùng có thể gây bệnh
địa phương cho dân cư [4].
Thực vật hấp thụ
F dưới dạng hòa tan trong đất. Khi độ
hòa tan của khoáng vật chứa F thấp thì F sẽ ít bị
rửa trôi bởi nước mưa, nhưng lại
tăng cao hàm lượng trong nước dưới đất,
và tạo điều kiện cho thực vật hấp thụ.
Do đó, trong thiên nhiên phần nào có sự cân bằng sinh
thái hàm lượng F trong nước và trong đất. Tuy
nhiên, sự cân bằng này có thể bị thay đổi
trong trường hợp xuất hiện những dạng
F dễ hấp thụ bởi động vật và thực
vật do hoạt động nhân sinh của con người.
Thí dụ, với hàm lượng trung bình của đạm
và kali trong đất thì lá cà chua tích luỹ 74 ppm, khi
tăng lượng phân đạm, hàm lượng F trong lá
tăng đến 540 ppm. Các công trình nghiên cứu đã công
bố cho thấy việc bón superphosphat đơn kéo dài 15
năm làm tăng hàm lượng F trong đất 22 %, trong
hạt 11 %, trong lá ngô tăng 1,4 lần, củ cải 1,6 lần.
Khi bón superphosphat cho đồng cỏ
với mức 250-500 kg/ha, hàm lượng F trong cỏ đạt
250-800 ppm [4].
Hàm lượng F trong thực vật rất thấp,
trung bình chỉ đạt 0,1-0,4 ppm. Hàm lượng F cao nhất
ghi nhận được trong rau khoảng 17-22 ppm, trong quả
đạt 0,1-0,72 ppm. Đặc biệt là ở lá chè, hàm
lượng F tới 57-1.370 ppm.
Bảng 2. Hàm lượng fluor (ppm) trong một
số thực phẩm [9]
|
TT |
Loại thực phẩm |
Hàm lượng F |
TT |
Loại thực phẩm |
Hàm lượng F |
|
1 |
Khoai lang |
8,62 |
8 |
Hành tây |
0,12 |
|
2 |
Cà chua |
0,5 |
9 |
Chuối tiêu |
0,23 |
|
3 |
Khoai tây |
0,5 |
10 |
Bưởi |
0,25 |
|
4 |
Cà rốt |
0,61 |
11 |
Dưa chuột |
0,2 |
|
5 |
Bột mỳ |
0,53 |
12 |
Súp lơ |
0,12 |
|
6 |
Nấm mỡ |
0,31 |
13 |
Cá trích |
0,16 |
|
7 |
Đậu tương |
14,7 |
14 |
Cá thu |
0,15 |
3. Fluor trong
nước
Môi trường nước là
nguồn cung cấp F chính và phổ biến nhất cho
cơ thể con người. Sự phân bố F trong nước
mặt, nước dưới đất và nước
khoáng nóng có sự khác biệt rõ ràng.
Nước biển
tương đối giàu F với hàm lượng 0,8-1,4
mg/l. Nước sông, nước ao hồ, nước giếng
có hàm lượng F thấp hơn khoảng 0,5 mg/l. Bởi
vậy, môi trường có ít Ca-HCO3-Na thì sẽ thuận
lợi cho việc tách F từ đá và tích tụ nó. Khi hàm
lượng Ca2+ tích tụ trong nước 0-25 mg/l
thì sự tập trung F có thể vượt 20 mg/l, nhưng
khi Ca2+ tăng đến 200 mg/l thì F tích tụ
<2,0 mg/l. Hàm lượng F thường tăng với sự
tăng độ pH của môi trường và hàm lượng
vật chất hữu cơ. Môi trường càng kiềm,
càng thuận lợi cho việc hoà tan và tích tụ F ở dạng
F-.
Kết quả khảo sát của Viện Vệ sinh
thành phố Hồ Chí Minh (1997) cho thấy hàm lượng F
trong nước sông Sài Gòn rất thấp, khoảng 0,025 -
0,13 mg/l. Kết quả phân tích bước đầu một
số nguồn nước ở đồng bằng Cửu
Long cho thấy, hàm lượng F rất nhỏ, hàm lượng
trung bình chỉ khoảng 0,02 - 0,6 mg/l, trong đó nhiều
vùng có hàm lượng F đạt dưới mức 0,1
mg/l (Bảng 3).
Theo kết quả đo vẽ, lập
bản đồ đẳng trị hàm lượng F
năm 1990 của Đoàn Địa chất Việt-Tiệp
thì tại các tỉnh Nam Trung Bộ, hàm lượng F trong
nước giếng thường nằm trong khoảng
2,5-3 mg/l, thậm chí có nơi như Đồng Xuân, Ninh
Thượng lên đến 9,4 mg/l và Ninh Hải là 13 mg/l.
Nguyên nhân được xác định là do sự thâm nhập
của nước khoáng, nước nóng có hàm lượng
F cao vào trong nước sinh hoạt, vì thấy có sự liên
hệ theo phương kéo dài và các vị trí giao thoa của
đứt gãy với các dị thường địa hóa
của F trong nước dưới đất.
Tài liệu khảo sát của Đặng
Trung Thuận [1], Đặng Trung Thuận và Đặng
Trung Tú [2] cho hàm lượng F trong nước mặt,
nước dưới đất vùng Ninh Hoà dao động
khoảng từ dưới 1 mg/l đến hơn 9 mg/l. Một
số nguồn nước khoáng nóng ở đây khá giàu F,
như nguồn nước nóng M’Dung thuộc xã Ninh Tây xuất
lộ từ khối granit thuộc phức hệ Định
Quán có hàm lượng F khá cao, khoảng 8,9-9,3 mg/l. Trong khi
đó, một số nguồn nước mặt có hàm
lượng F không cao, như nước sông Cái, sông Lốt,
hồ Đá Bàn chỉ khoảng 0,11-0,26 mg/l. Nước giếng
trong vùng có hàm lượng F dao động trong khoảng
0,1-6,8 mg/l, tức là từ rất thấp đến rất
cao, trong đó có 10/22 giếng nước có hàm lượng
F nhỏ hơn 1 mg/l và 8/22 giếng nước có hàm lượng
lớn hơn 1,5 mg/l. Hành vi địa hóa của F ở
đây liên quan chặt chẽ với sự phân bố của
các nguyên tố Ca, Mg và độ pH của nước. Hệ
số tương quan có ý nghĩa của F-Ca là -0,49, F-Mg là
-0,35, F-pH là 0,75. Điều này thể hiện hai nguyên tố
Ca và Mg kết hợp với F tạo thành CaF2 và MgF2
là các chất khó hòa tan.
Bảng 3.
Hàm lượng (ppm) của F trong nước sinh hoạt
vùng đồng bằng Cửu Long [14]
|
STT |
Địa phương |
Hàm lượng |
S TT |
Địa phương |
Hàm lượng |
|
1 |
Cầu Bến Lức,
Long An |
0,07-0,08 |
7 |
TX. Rạch Giá,
Kiên Giang |
0,18 |
|
2 |
TX. Sóc Trăng |
0,09 |
8 |
TX. Hà Tiên, Kiên
Giang |
0,6 |
|
3 |
Tân Châu, An Giang |
0,06 |
9 |
TX. Cao Lãnh, Đồng
Tháp |
0,05-0,1 |
|
4 |
Mỹ Tho, Tiền
Giang |
0,02 |
10 |
TX. Cà Mau |
0,27 |
|
5 |
Cái Bè, Tiền
Giang |
0,02 |
11 |
TX. Bến Tre |
0,19-0,4 |
|
6 |
Gò Công, Tiền
Giang |
0,35 |
12 |
TX. Vĩnh Long |
0,07 |
V. VAI TRÒ CỦA
FLUOR ĐỐI VỚI SỨC KHỎE CỘNG ĐỒNG
Kiểm soát hàm lượng của F trong môi trường
là một vấn đề quan trọng đối với
sức khỏe cộng đồng. Bởi nếu cơ thể
con người hấp thụ quá nhiều hoặc quá ít F từ
môi trường đều dẫn đến những tác
động có hại cho sức khỏe. Ở nước ta,
từ 1985 đến nay đã có nhiều tiêu
chuẩn về giới hạn hàm lượng fluor áp
dụng cho nước uống, cho nước mặt
và nước dưới đất phục vụ cấp
nước làm cơ sở cho việc đánh
giá mức độ ô nhiễm nguồn
nước (giới hạn tối đa hàm lượng
fluor là 1,5 mg/l) (Bảng 4).
Bảng 4. Giá
trị giới hạn của hàm lượng fluor trong
nước
|
Tiêu
chuẩn |
Giới
hạn tối đa (mg/l) |
|
|
TCN 33-85BXD |
0,7
- 1,5 |
|
|
TCVN 5501-1991 (nước uống) |
0,7
- 1,5 |
|
|
TCVN 5501-1991 (chất lượng
nước dưới đất phục vụ cấp
nước) |
Mức chấp nhận |
Mức mong muốn 0,75 |
|
TCVN 505BYT/QĐ-1992 (nước
cấp cho ăn uống và sinh hoạt) |
Giới hạn tối đa 1,5 |
|
|
TCVN 5942-1995 (chất lượng
nước mặt) |
1 - 1,5 (tùy mục đích sử
dụng) |
|
|
TCVN 5944-1995 (chất lượng
nước dưới đất) |
1,0 |
|
|
TCXD 233-1999 (nguồn nước
mặt và nước dưới đất phục vụ
cấp nước) |
0,5 - <1,5 |
|
|
TCYT 1329/2002/BYT/QĐ (nước
cấp cho ăn uống) |
0.7 - 1,5 |
|
Fluor hấp thụ vào cơ thể con người chủ
yếu qua nước uống và thức ăn. Đối
với một số người hoạt động trong
lĩnh vực công nghiệp có sử dụng hóa chất của
F (luyện kim, điện tử…), F có thể thâm nhập
vào máu qua con đường hô hấp và qua da. Fluor có thể
hấp thụ rất nhanh vào máu.
Fluor có thể ức chế
hoạt hoá chức năng một số men tiêu hoá, làm
tăng khả năng hoạt động của
andenylcyclas và nhiều hocmon khác. Fluor kích thích tổng hợp
collagen ở giai đoạn đầu khôi phục vị
trí gãy xương. Chính vì vậy, cơ thể động
vật nói chung, và con người nói riêng, dùng F vào việc
hoàn chỉnh xương móng, sừng và hệ thần kinh.
Fluor còn ảnh hưởng đến trao đổi
phosphor-calci, hoạt tính của các enzym. Tác dụng chống
sâu răng của F là do khả năng của nó ức chế
các enzym hỗ trợ sự sinh sản của các vi khuẩn
miệng, và khả năng liên kết với các ion calci, nhờ
đó giúp tăng cường men răng đang hình thành ở
trẻ em. Qua nghiên cứu, người ta còn phát hiện
được NaF có vai trò kích thích trực tiếp các tế
bào xương, dẫn đến sự tăng khả
năng hình thành xương, tránh các bệnh loãng
xương. Nhưng ở liều lượng nào đó F lại
có thể gây rối loạn về độ khoáng hoá
xương. Người ta cũng còn biết, sự dư
thừa NaF trong cơ thể dẫn đến hiện
tượng cao huyết áp.
Khối lượng F mà cơ thể hấp thụ
không chỉ phụ thuộc vào khối lượng F
đưa vào cơ thể, thời gian tiếp xúc, tần
suất tiếp xúc, nồng độ tiếp xúc mà còn phụ
thuộc vào giới tính, độ tuổi và tình trạng sức
khỏe của cơ thể. Hàm lượng F trung bình mà một
cơ thể trưởng thành hấp thụ từ thức
ăn và nước uống ước tính khoảng 1 mg nếu
sống trong vùng mà nước uống có hàm lượng F
dưới 0,7 ppm, và khoảng 2,7 mg, nếu nước uống
được bổ sung F.
F được bài tiết qua con đường tiêu
hoá (10% qua phân), mồ hôi (25-40 %), sữa (không đáng kể),
nước bọt < 1 % và chủ yếu là qua con
đường nước tiểu. Sau khi thâm nhập vào
cơ thể, khoảng một nửa hàm lượng F sẽ
bị đào thải rất nhanh ra khỏi cơ thể
qua con đường bài tiết, thông thường là khoảng
24 giờ, ngoại trừ khi hấp thụ với hàm
lượng lớn (từ 20 mg trở lên). Một phần
F sẽ bị giữ lại trong cơ thể và tích lũy
ở trong xương và răng.
VI. TÌNH HÌNH Ô NHIỄM
FLUOR VÀ CÁC BỆNH LIÊN QUAN Ở VIỆT
Tuy đã có những nghiên cứu riêng lẻ nhưng
đến nay ở Việt Nam chưa có những công trình
điều tra một cách hệ thống sự phân bố
của F trong các thành phần của môi trường tự
nhiên và đánh giá những tác động bất lợi của
môi trường dư thừa hoặc thiếu hụt F tới
sức khỏe và sự phát triển của cộng đồng
cư dân.
Một số công trình nghiên cứu đề cập ở
trên đã chỉ ra rằng ở Việt Nam có những vùng
rất nghèo F như đồng bằng Cửu Long và Hà Nội.
Kết quả phân tích bước đầu một số
nguồn nước ở đồng bằng Cửu Long
cho thấy, hàm lượng F rất nghèo, dưới mức
quy định về an toàn vệ sinh, hàm lượng trung
bình chỉ khoảng 0,02 - 0,6 mg/l, trong đó nhiều khu vực
có hàm lượng F đạt dưới mức 0,1 mg/l, có
khả năng tiềm ẩn nguy cơ thiếu hụt F
trong môi trường.
Hàm lượng F trong nguồn nước ăn uống
ở Hà Nội cũng rất thấp, chỉ khoảng 0,1
- 0,3 mg/l nhưng chưa đánh giá được mức
độ tác động tới sức khỏe. Các tỉnh
còn lại còn ít có số liệu điều tra. Qua kết
quả khảo sát dịch tễ học ở Thái Bình cho thấy
trong cộng đồng dân cư thấy biểu hiện bệnh
địa phương của F như răng có đốm
nâu và trắng đục. Vấn đề này cần có sự
kiểm tra tiếp theo.
Các bệnh địa phương liên quan đến
việc nhiễm độc F ở các tỉnh Nam Trung Bộ
gần đây đã được chú ý. Những khu vực
này phân bố rải
rác ở Ninh Thọ - Vạn Ninh, Ninh Hòa, bờ phải
sông Trầu, Sơn Thai, Khánh Thượng - Khánh Vĩnh, Cam
Hiệp Bắc, Cam Hiệp Đông và Cam Ranh. Ở những
nơi này, nước ngầm có hàm lượng F tối
thiểu là 1,5 mg/l. Tại Ninh Hòa có tới 11 xã bị nhiễm
F trong nước giếng bao gồm: Ninh Tây, Ninh Xuân, Ninh
Thượng, Ninh Bình, Ninh Quang, Ninh Phụng, Ninh Thân, Ninh
Trung, Ninh Đông, Ninh Hải, Ninh Hà. Bệnh
hỏng răng do nhiễm F đã xuất hiện trên quy mô
rộng với các biểu hiện răng bị hỏng
men, biến thành màu nâu hay đen xỉn, sứt mẻ, siêu
vẹo nên được gọi là “vùng đất không có nụ
cười”. Có thể bệnh này còn phổ biến ở
nhiều nơi khác của miền Nam Trung Bộ vì tại
đây có rất nhiều nguồn khoáng nóng có chứa F với
hàm lượng cao, phổ biến khoảng 2-8 mg/l, và có thể
đạt tới 10-12 mg/l [6].
Kết quả điều tra của ngành Y tế Khánh
Hoà về số người mắc bệnh thừa-thiếu
fluor ở Ninh Hòa đã phát hiện được trên 76%
dân số mắc bệnh. Trong 8 xã điều tra thì có 3 xã
có tỷ lệ mắc bệnh hơn 90 %, 2 xã hơn 80 %, một
xã hơn 79 % và 2 xã hơn 60 %. Tỷ lệ người mắc
bệnh cao nhất là Ninh Xuân (96,53%), và thấp nhất là
Ninh Sim (67,05 %) (Bảng 5). Số người nhiễm bệnh
giảm theo chiều tăng của độ tuổi (Hình
2), và ở độ tuổi dưới 15 có số lượng
nhiễm bệnh cao nhất, chiếm 41,63 % số người
mắc bệnh. Ở Cam Ranh, tại thôn Tà Long (Ba Ngòi) kết
quả điều tra năm 1999 trên 398 hộ với 250 giếng
nước đã phát hiện 65 % giếng nước nhiễm
F và 82 % số người có biểu hiện bị bệnh
hỏng răng do nhiễm F.
Các kết quả này cũng cho thấy
hàng trăm hộ dân ở làng Quế Châu, xã Nhơn Tân, huyện
An Nhơn, Bình Định mắc bệnh răng đen. Một
cuộc khảo sát mới đây của Viện Răng hàm
mặt TP Hồ Chí Minh đối với 44 trẻ em ở
đây cho thấy 100% trường hợp đều bị
mắc bệnh về fluor nặng và rất nặng.
Đáng lưu ý là hàm lượng F trong mỗi lít nước
lên tới 6,6 mg.
Bảng 5. Kết quả điều tra về số
người mắc bệnh thừa-thiếu fluor ở Ninh
Hòa
|
TT |
Xã |
Số hộ |
Số nhân khẩu |
Số người mắc bệnh |
Tỷ lệ (%) |
<15 |
15-19 |
20-29 |
30-44 |
45-64 |
|
1 |
Ninh Hương |
238 |
1130 |
1044 |
92,39 |
397 |
211 |
129 |
207 |
100 |
|
2 |
Ninh Bình |
175 |
961 |
648 |
67,43 |
202 |
136 |
173 |
97 |
40 |
|
3 |
Ninh Quang |
105 |
505 |
422 |
83,56 |
168 |
73 |
106 |
45 |
30 |
|
4 |
Ninh Thân |
98 |
542 |
424 |
78,23 |
153 |
82 |
125 |
52 |
12 |
|
5 |
Ninh Sim |
97 |
525 |
352 |
67,05 |
147 |
79 |
88 |
38 |
0 |
|
6 |
Ninh Trung |
161 |
883 |
748 |
84,71 |
296 |
128 |
157 |
98 |
69 |
|
7 |
Ninh Xuân |
437 |
1383 |
1335 |
96,53 |
527 |
396 |
251 |
131 |
30 |
|
8 |
Ninh Phụng |
231 |
1064 |
966 |
90,79 |
374 |
153 |
214 |
134 |
91 |
|
|
Tổng |
1542 |
7093 |
5439 |
76,68 |
2264 |
1258 |
1234 |
802 |
327 |
Nguồn: Sở Y tế tỉnh
Khánh Hòa, 1999
|
|
Hình 2. Đồ thị biểu diễn
số người mắc bệnh về fluor theo độ
tuổi
Các đá granitoid thuộc các phức
hệ có tuổi khác nhau ở một số vùng thuộc
các tỉnh Phú Yên và Khánh Hòa đã được phát hiện
là chứa nhiều mạch khoáng hóa fluorit, có nơi tập
trung thành mỏ fluorit như mỏ Phú Mỡ, mỏ Xuân Lãnh
(huyện Đồng Xuân, Phú Yên). Ở những nơi này,
dân uống nước bị nhiễm F nên thường mắc
bệnh mủn răng [5].
VI. MỘT SỐ BIỆN PHÁP GIẢM
THIỂU BỆNH ĐỊA PHƯƠNG DO FLUOR
1. Những
nơi thiếu fluor
Cần áp dụng các biện pháp làm tăng
một cách có kiểm soát hàm lượng fluor trong khẩu
phần thức ăn. Một trong đề xuất
này là việc trộn fluor vào trong muối ăn. Lạng
Sơn là một trong những tỉnh đầu tiên thử
nghiệm sử dụng muối trộn fluor. Khi sử dụng
rộng rãi, loại muối này sẽ giảm đáng kể
bệnh sâu răng, căn bệnh mà có tới 75-90% người
Việt
Khi nguồn nước còn thiếu fluor, một
trong những cách cách phòng sâu răng tốt nhất là bổ
sung vào nước cho đạt tới mức tối
ưu. Tuy nhiên, 80% dân số ở nông thôn không có nước
máy, nên việc bổ sung fluor qua nước máy cũng chỉ
đến với 20% người dân. Trong khi đó, muối
là gia vị hàng ngày của bất cứ gia đình nào. Fluor
phải được trộn vào muối theo đúng hàm
lượng, tỉ lệ được WHO khuyến cáo
là 250 mg/kg muối và Lạng Sơn sẽ là một trong những
địa phương đầu tiên thử nghiệm
chương trình này.
Chế độ thức ăn hàng ngày cũng cần
được lưu ý, vì hàm lượng fluor gây tác hại
mạnh khi trong thành phần thức ăn thiếu các chất
cần thiết như: Ca, Mg, vitamin C từ rau và các loại
trái cây.
2. Những
nơi dư thừa fluor
Có thể dùng một số biện
pháp như dùng sét, các khoáng chất thích hợp, một số
loại nhựa trao đổi ion, than hoạt tính, nhôm hoạt
tính, than sulfonic hóa và serpentin để tách hàm lượng F
vượt tiêu chuẩn môi trường ra khỏi nước.
Việc xử lý hóa học tại chỗ bằng vôi, muối
magnesi cũng có kết quả trong việc khử F. Tuy vậy,
tất cả các biện pháp này đều vấp phải
một số trở ngại nhất định là giá thành
cao, năng suất khử F thấp, hóa chất đem xử
lý còn thiếu tính chọn lọc đối với F và việc
phục hồi lại hóa chất rất phức tạp hoặc
tốn kém.
Như phần trên đã đề
cập, vật cản địa hóa chính của F là Ca và
Al. Khi F kết hợp với Ca tạo thành CaF2 và với Al
tạo thành AlF3, hai chất này có tích số hòa tan nhỏ sẽ
kết tủa xuống. Vì vậy, có thể sử dụng
các hợp chất dễ tan có chứa hai nguyên tố này làm
chất khử F trong nước sinh hoạt. Sau đây xin
giới thiệu một số giải pháp công nghệ xử
lý fluor trong môi trường nước:
a. Nếu
hàm lượng fluor trong nước cấp < 0,5 mg/l: Cần phải fluor hóa nguồn nước bằng
cách bổ sung lượng F cần thiết vào nước.
Các chất có thể được dùng như fluorur silic
natri, fluorur natri, fluorur silic ammoni.
Liều lượng hóa chất đưa vào
được tính theo công thức :

trong đó: a –
Hàm lượng F cần thiết trong nước xử lý,
a = 0,7 - 1,2 g/m3;
Fhc – Hàm
lượng F trong hóa chất tinh khiết phụ thuộc
vào loại hóa chất sử dụng: fluorur silic natri - Fhc
= 60; fluorur natri - Fhc = 45; fluorur silic ammoni : Fhc =
64
F0 - Hàm
lượng F có trong nước nguồn (g/m3);
Cfluor -
Hàm lượng hóa chất tinh khiết trong sản phẩm
(%);
b. Nếu hàm lượng fluor trong
nước lớn hơn giới hạn cho phép (> 1,5 mg/l): Một trong những phương pháp kinh tế nhất
để xử lý F là kết tủa với nước
vôi và CaCl2 với phương trình phản ứng
như sau: 2 F- + Ca2+ → CaF2
Phương pháp
này dựa trên việc tạo thành chất ít tan CaF2
theo phương trình: Ca(OH)2 + 2 HF → CaF2
+ 2 H2O.
Kết tủa này có thể
tách khỏi dung dịch bằng chất làm đặc và lọc
gạn. Bùn lọc có thể xử lý như những loại
bùn khác, loại nước bằng lọc chân không hoặc
ly tâm. Giới hạn của phương pháp này là độ
tan của fluorur calci là 7,8 mg/l (tính theo F). Để có thể
tăng hiệu quả có thể thêm sulfat magnesi vào dung dịch
hoặc sử dụng nước vôi dolomit.
+ Sử dụng
oxit nhôm Al2O3: Là công nghệ do PGS.TS Nguyễn Văn
Phước, Đại học Bách Khoa TP HCM nghiên cứu
năm 2007 [11]. Hoá chất sử dụng là oxit nhôm hoạt
tính do công nghiệp sản xuất.
Quy trình xử lý
F bằng oxit nhôm hoạt tính là phương pháp được
lựa chọn tại các nước phát triển. Oxit nhôm
hoạt tính có khả năng hấp thụ F rất cao. Vật
liệu hấp thụ dạng hạt như oxit nhôm hoạt
hóa Al2O3 làm lớp vật liệu lọc
cho bể lọc xử lý F. Oxit nhôm hoạt tính dùng để
xử lý nước thường có cấu trúc vô định
hình với kích thước 0,3-0,6 mm đường kính. Khả
năng hấp thụ tốt nhất ở pH < 8,2. Quá
trình hấp phụ F- trên oxit nhôm hoạt tính ngoài hấp
phụ vật lý còn có quá trình trao đổi ion, trao đổi
OH bề mặt oxit nhôm như sau:

Gần đây, Nguyễn
Bá Trinh thuộc Viện Khoa học và Công nghệ Việt
Nam đã nghiên cứu và chế tạo thành công hợp chất
lọc nước DS-3. DS-3 là hỗn hợp khoáng và chất
hữu cơ có nguồn gốc sinh học, nên an toàn cho
người sử dụng và môi trường. DS-3 có tác dụng
lọc tổng hợp được chế tạo để
xử lý nhiều nguồn nước cấp khác nhau thành
nước sinh hoạt đạt tiêu chuẩn vệ sinh.
Trên đây là một số
biện pháp đơn giản để xử lý các nguồn
nước nhiễm F phù hợp với điền kiện
của Việt Nam. Tuy nhiên, ngoài các biện pháp nêu trên, để
hạn chế tác hại của nước nhiễm F còn cần
chú ý đến các biện pháp giáo dục và chăm sóc sức
khỏe cộng đồng. Khuyến cáo người dân
trong vùng không nên sử dụng các loại kem đánh răng
và các sản phẩm vệ sinh răng, đồ uống
các loại không bổ sung F, hạn chế uống trà và các
thực phẩm có chứa nhiều F, đồng thời
thay đổi cơ cấu trong khẩu phần ăn bằng
cách bổ sung các chất Ca, Mg (sữa calci, các động
vật giáp xác,...) và vitamin C (rau xanh và các loại hoa quả).
KẾT LUẬN
Fluor được sinh ra từ nhiều
nguồn (tự nhiên và nhân tạo), chủ yếu là nguồn
tự nhiên thông qua các quá trình hoạt động địa
chất như: quá trình nhiệt dịch liên quan với các
đá magma, hoạt động núi lửa cổ và hiện
đại, hoạt động của nước dưới
đất và các điểm nước khoáng nóng kiềm,
quá trình phong hoá trên các đá và các khu mỏ chứa F.
Fluor có hoạt tính hóa học mạnh, độ linh
động cao. Sự tồn tại của F trong môi
trường phụ thuộc vào điều kiện môi
trường và mối tương tác (có quy luật hoặc
không rõ quy luật) với các nguyên tố khác. Với calci và
nhôm, F có tương quan chặt chẽ trong đất cũng
như trong nước. Calci và nhôm được coi là vật
cản địa hóa chủ yếu của F. Ngoài ra, F
thường kết hợp với các nguyên tố hoá học
khác trong các khoáng vật ở các tụ khoáng.
Sự phân bố và hành vi của F trong các môi trường
đá, đất, thực vật, vỏ phong hoá và nước
rất khác biệt, trong đó, môi trường nước
là nguồn cung cấp F chính và phổ biến nhất cho
cơ thể con người thông qua chuỗi thức
ăn. Sự phân bố F trong nước mặt, nước
dưới đất và nước khoáng nóng cũng có sự
khác biệt rõ ràng.
Theo tiêu chuẩn vệ
sinh nước ăn uống của Bộ Y tế
(1329/2002/BYT/QĐ) [10] Hàm lượng F chấp nhận
được là 0,7 mg/l < F < 1,5 mg/l. Việc thiếu
hay thừa F trong cơ thể đều có tác động
đến răng và xương. Thừa F trong cơ thể
có thể gây bệnh thừa-thiếu fluor (đối với
răng và xương). Ngoài ra, thừa F trong cơ thể
còn có thể làm suy giảm hoạt động của tuyến
giáp, gây tổn thương tới não, sinh các trẻ mắc
bệnh hội chứng “down” ở phụ nữ.
Ở Việt
Nam có một số địa phương bị thiếu
hụt F trong nước dưới đất như Hà Nội,
trong nước dưới đất và nước mặt
ở đồng bằng Cửu Long. Hàm lượng F trong
các loại thực phẩm ở Việt Nam nhìn chung đều
thấp. Trong khi đó, các vùng có sự dư thừa F trong
nước dưới đất điển hình là Vạn
Ninh, Ninh Hòa, Cam Ranh (tỉnh Khánh Hòa) và một số vùng khác
của các tỉnh Thái Bình, Bình Định và Ninh Thuận.
Nguyên nhân của sự dư thừa F trong nước
được xác định là do sự thâm nhập của
các nguồn nước khoáng, nước nóng có hàm lượng
F cao vào nước dưới đất. Ngoài ra, còn có thể
liên quan đến các mạch nhiệt dịch giàu các khoáng
vật chứa F.
Các vùng có sự thiếu hụt F trong môi trường
cần phải được nghiên cứu kỹ hơn
để đưa ra hàm lượng hợp lý của F
để bổ sung vào khẩu phần ăn và nước
uống hàng ngày sao cho đạt được giới hạn
hấp thụ 1 mg/người/ngày.
Đối với các vùng có sự dư thừa F trong
môi trường, cần có sự điều tra đánh giá
một cách hệ thống trạng thái môi trường
để đề xuất các biện pháp tối ưu.
Những vùng này có thể áp dụng một số
phương pháp đơn giản, như sử dụng hợp
chất DS-3, oxit nhôm hoạt tính để xử lý loại
bỏ hàm lượng F dư thừa kết hợp với
các biện pháp giáo dục và chăm sóc sức khỏe cộng
đồng khác.
Để có thể áp dụng biện pháp bổ sung hoặc
loại bỏ F trong nước sinh hoạt, thực phẩm
như nêu ở trên, một nghiên cứu tổng thể nhằm
đánh giá hành vi địa hóa và sự phân bố tự
nhiên của F trong môi trường địa chất là cần
thiết và cần sớm triển khai. Kết quả nghiên
cứu này sẽ là cơ sở khoa học giúp quy hoạch
định hướng chương trình fluor hóa muối
ăn tầm quốc gia, phù hợp với từng vùng
địa hóa hoặc đới địa bệnh nguyên
khác nhau trên lãnh thổ Việt Nam.
VĂN LIỆU
1. Đặng Trung Thuận, 2000. Điều tra địa hóa môi trường vùng
Ninh Hòa, tỉnh Khánh Hòa. Lưu trữ Tổng hội
Địa chất Việt
2. Đặng Trung Thuận,
Đặng Trung Tú, 2008. Ô nhiễm fluor và bệnh chết răng ở Nam Trung
Bộ. TC Địa chất,
A/309 : 41-50. Hà Nội.
3. Đỗ Thị Vân Thanh,
Đặng Trung Thuận, Nguyễn Ngọc Trường,
Nguyễn Thị Thanh Lan, Nguyễn Văn Dục, 2002. Ô nhiễm fluor trong nước sinh hoạt ở
Phú Yên và bệnh fluorit ở Đồng Xuân, Phú Yên. Lưu
trữ Trường ĐH
Khoa học Tự nhiên, ĐHQG. Hà Nội.
4. Đỗ Văn Ái, 2002. Những bệnh địa phương liên quan với
fluor trong môi trường. Thông tin KHKT ĐC. Loạt chuyên
đề “Những vấn đề địa chất
sinh thái”. Tập IV. Địa chất y học. Trung tâm
Thông tin Lưu trữ ĐC, Hà Nội.
5. Nguyễn
Đình Hòe, 2000. Vùng đất không có nụ cười. Báo Khoa học
và đời sống, 1341. Hà Nội.
6. Nguyễn Hoàng Liên, Nguyễn
Phương Lan, Lưu Đức Hải, 1998. Vai trò của các nguyên tố hóa học trong quá
trình dinh dưỡng của con người. Thông tin
KHKT ĐC. Loạt chuyên đề
“Những vấn đề địa chất sinh thái”.
7. Nguyễn
Hồng Quang, 2007. Điều tra đánh giá hiện trạng, nguồn gốc
và khả năng di chuyển dị thường một số
nguyên tố (F, As, Hg) dải ven biển Bình Định -
Ninh Thuận, ảnh hưởng của chúng tới sức
khỏe cộng đồng và đề xuất giảm nhẹ
hậu quả. Lưu trữ Viện KH Địa chất
và Khoáng sản. Hà Nội.
8. Phạm Song, Nguyễn Bá Trinh,
Vũ Văn Hiển, 1996. Công
nghệ cung cấp nước sạch và vệ sinh môi
trường. Nxb Khoa học và kỹ
thuật. Hà Nội.
9. Phạm
Thị Thục, 2000.
Vai trò của vi chất fluor đối với sức khỏe
con người. Ykhoanet.com website. Url:
http://home.ykhoa.net/thuocmen/27_124.htm
10. Tiêu chuẩn Việt Nam, 2001. Yêu cầu kỹ thuật
nước uống, nước sinh hoạt và
phương pháp thử. Nxb
Xây dựng, Hà Nội.
11. Trường Đại học Khoa học
TP Hồ Chí Minh, 2007.
Báo cáo tóm tắt Đề tài: “Nghiên cứu xử lý hàm
lượng fluor trong nguồn nước ngầm bị ô
nhiễm tại khu vực các xã Bình Tường, Tây Giang
(huyện Tây Sơn) và Nhơn Tân (huyện An Nhơn) tỉnh Bình Định”. Lưu trữ
ĐHKH, TP Hồ Chí Minh.
12. Vinogradov A.P. (Ed.) 1967. Chemistry of the Earth's crust. Vol. 1 & Vol. 2. Publisher of
13. Võ Công Nghiệp, 2002. Khái niệm về những dị thường
địa sinh thái và ảnh hưởng của chúng đến
sức khỏe con người và giới sinh vật. Thông
tin KHKT ĐC. Loạt chuyên đề “Những vấn đề
địa chất sinh thái”. Tập IV: Địa chất y
học. Trung tâm Thông tin Lưu trữ ĐC, Hà Nội.
14. Võ Thế
Quang, 1985. Phòng bệnh
sâu răng bằng fluor. Nxb Y học, TP Hồ Chí Minh.
15. Vũ Ngọc Trân,
2002. Ảnh
hưởng xấu của các dị thường địa
sinh thái và một số vấn đề địa chất
y học ở tỉnh Khánh Hòa. Thông tin KHKT ĐC. Loạt
chuyên đề “Những vấn đề địa chất
sinh thái”. Tập IV: Địa chất y học. Trung tâm Thông tin Lưu trữ
ĐC, Hà Nội.